Базовая организация - Институт физиологически активных веществ Федерального государственного бюджетного учреждения науки Федерального исследовательского центра проблем химической физики и медицинской химии
Российской академии наук (ИФАВ РАН)
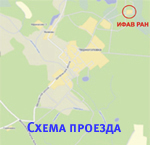
Адрес: 142432 Московская обл., г. Черноголовка, Северный проезд, д. 1
| 01 |
Оценка влияния соединений на полимеризацию тубулина |
| 02 |
Получение и культивирование больших количеств ранних эмбрионов мыши с помощью гормональной стимуляции суперовуляции и синхронного выброса |
| 03 |
Хирургическая трансплантация ранних эмбрионов самкам-реципиентам после создания необходимого гормонального фона |
| 04 |
Ведение и размножение линий трансгенных мышей, содержащих регулируемые CRE-рекомбиназы, с обязательным регулярным анализом копийности трансгенной кассеты методом ПЦР в реальном времени |
| 05 |
Выделение микротубулярных белков из мозговой ткани грызунов (крыс и мышей) |
| 06 |
Исследование токсичности при многократном 28-дневном пероральном введении на грызунах |
| 07 |
Определение класса острой токсичности при пероральном введении |
| 08 |
Исследование острой токсичности при пероральном введении, процедура фиксированной дозы (Fixed dose procedure, FDP) |
| 09 |
Поведенческое фенотипирование модельных животных в лабиринте Мориса |
| 10 |
Оценка влияния на олигомеризацию и образование фибрилл амилоидных пептидов флуориметрическим методом |
| 11 |
Определение цитотоксичности веществ МТТ-тестом на культуре нормальных клеток млекопитающих MDSK-M |
| 12 |
Определение цитотоксичности веществ МТТ-тестом на культуре нормальных клеток человека HEK293 |
| 13 |
Стереоскопические операции на головном мозге мышей для адресного введения в заданные анатомические области мозга нейротоксинов и генноинженерных конструкций (в том числе лентивирусных и аденовирусных) с целью получения экспериментальных моделей нейродегенеративных заболеваний |
| 14 |
Контроль рекомбинации в геноме, активированной тамоксифеном, путем анализа активности реферного гена (бета галактозидазы) в локусе ROSA на шестой хромосоме |
| 15 |
Анализ корректности рекомбинации в геноме, активированной тамоксифеном, с помощью генетического анализа фланкированных участков ДНК |
| 16 |
Оценка определения состояния специфических нейроинфламматорных реакций у модельных животных по каждому из следующих маркеров: RCAI, Iba1 (микроглиоз), GFAP (астроглиоз) |
| 17 |
Создание модельных линий мышей, содержащих заданный набор модификаций генома, необходимых для регулируемой тканеспецифической инактивации генов (обязательно использование в коровых линиях флакирующих сайтов для CRE или FRT рекомбинации; рекомбиназы в составе трансгенных кассет должны быть конъюгированными с эстрагеновым рецептором и активироваться тамоксифеном) |
| 18 |
Поведенческое фенотипирование модельных животных в камерах для оценки походки |
| 19 |
Высокопроизводительный скрининг in vitro оценки влияния соединений на функции митохондрий с использованием теста определения кальций-индуцированного набухания изолированных митохондрий |
| 20 |
Высокопроизводительный скрининг in vitro оценки влияния соединений на митохондриальный потенциал |
| 21 |
Высокопроизводительный скрининг in vitro оценки влияния соединений на кальциевую ёмкость митохондрий |
| 22 |
Высокопроизводительный скрининг потенциальных нейропротекторных препаратов по способности блокировать развитие эксайтотоксичности и токсического действия бета-амилоидного пептида |
| 23 |
Оценка влияния соединений на активность рекомбинантной киназы GSK 3 β по отношению к стандартному субстрату либо по отношению к рекомбинантному тау-протеину |
| 24 |
Оценка токсичности соединений для нормальных клеток |
| 25 |
Оценка эффективности исследуемых соединений на оригинальных клеточных (in vitro) и трансгенных животных (in vivo) моделях нейродегенеративных заболеваний человека |
| 26 |
Обеспечение исследований генно-модифицированными линиями животных (грызуны) |
| 27 |
Доклинические исследования в полном объеме новых потенциальных лекарственных средств в соответствии с правилами надлежащей лабораторной практики (GLP) и с использованием животных СПФ-статуса |
| 28 |
Оценка острой токсичности - на двух видах животных, при двух способах введения, с проведением морфологических исследований |
| 29 |
Изучение субхронической и хронической токсичности |
| 30 |
Изучение мутагенности |
| 31 |
Изучение иммунотоксичности |
| 32 |
Изучение аллергенности |
| 33 |
Изучение репродуктивной активности |
| 34 |
Оценка канцерогенной опасности |
| 35 |
Фармакокинетика |